Utsettelse for metamfetamin og kronisk sykdom hos politibetjenter: Signifikant forbedring med badstubasert avgiftningsterapi
OVERORDNET SAMMENDRAG
Abstrakt
Bakgrunn: Den medisinske litteraturen rapporterer om helserisiko for politifolk ved gjentatt utsettelse for metamfetamin og relaterte kjemiske sammensetninger. De fleste virkningene synes å være forbigående, men noen politibetjenter fra Utah med jobbrelatert utsettelse for metamfetamin, utviklet kroniske symptomer, noen førte til tapt funksjonsevne. Denne rapporten stammer fra en ikke-kontrollert, retrospektiv journalevaluering av politibetjenter med symptomer, behandlet med en badstubasert avgiftningsprosedyre med den hensikt å redusere de kroniske symptomene og forbedre livskvaliteten. Metoder: Sekstini politibetjenter, som etter tur deltok i Utah Meth Cops Project, ble vurdert før og etter et behandlingsprogram som omfatter gradvis økende mosjon, omfattende kosttilskudd og fysisk badstuterapi. Evalueringer inkluderer poengresultat fra Research and Development Corporation (RAND) før og etter behandlingen. Short Form Health Survey (SF-36) med trettiseks poster, sammenlignet med RAND-normer for befolkningen, poengintensitet for symptomer før og etter behandling, nevrotoksisitet, Mini-Mental Status Examination, presenterer symptomhyppighet og en strukturert evaluering av hvor trygt behandlingsprogrammet er. Resultater: Statistisk signifikante helseforbedringer ble observert i SF-36-evalueringene, symptom-poengtall og nevrotoksisitet-poengtall. Avgiftningsprosedyren ble tålt godt, med en fullføringsrate på 93,8 %. Konklusjoner: Denne undersøkelsen antyder sterkt at bruk av badstue og kostholdsterapi kan lindre kroniske symptomer som viser seg etter å ha vært utsatt for kjemisk påvirkning forbundet med lovhåndhevingsaktiviteter der metamfetamin er involvert. Denne rapporten har også relevans når det gjelder å ta fatt i de åpenbart uheldige virkningene fra annen eksponering for komplekse kjemikalier. Med tanke på de positive kliniske utfallene i denne gruppen, synes mer omfattende undersøkelser av denne badstubaserte kuren å være berettiget.
Introduksjon
Personer som er avhengige av metamfetamin, utvikler alvorlige helseproblemer, men mindre forståelse omgir det store antallet lovens håndhevere som opplever signifikante symptomer forbundet med etterforskning av skjulte metamfetamin-laboratorier, (CDC 2005). Selv om symptomer kan være midlertidige, har mange personer standhaftige symptomer som får dem til å oppsøke lege.
Det å gripe inn mot et aktivt laboratorium har vært forbundet med en 7 til 15 ganger så stor risiko for å bli syk, sammenlignet med andre aktiviteter med åpenbart lavere kjemisk eksponering. Ifølge Marshall (2000), siden 1993 «har antallet etterforskninger av hemmelige stofflaboratorier fortsatt å stige, noe som gjør Utah til delstat nummer en når det gjelder metamfetamin-laboratorier per innbygger».
I 2007 undersøkte påtalemyndigheten i Utah et badstubasert avgiftningsprogram som opererte på Manhattan, med behandling av kronisk syke redningsarbeidere som hadde blitt utsatt under 11. september 2001, da World Trade Center ble angrepet og kollapset. En overordnet politimann og en profesjonell brannmann, som begge ble syke etter metamfetaminlaboratorie-relaterte eksponeringer i Utah, tilskrev vesentlig helseforbedring til det å ha mottatt denne behandlingen.
Den ideelle American Detoxification Foundation (ADF) etablerte og administrerte Utah Meth Cops Project (UMCP), som bruker Hubbard avgiftningsprosedyre og overvåker helsen og livskvaliteten blant Utahs politifolk, for å gripe fatt i symptomene som stemmer overens med (og viser seg etter) utsettelsen for metamfetamin og relaterte kjemikalier, de som gjorde sin plikt på post opplevde.
METODOLOGI:
Beskrivelse av studiegruppen, kriterier for inkludering og utelukking.
Dette er en retrospektiv journalevaluering av de første 69 politifolkene som etter tur begynte på UMCP mellom oktober 2007 og juli 2010. Politibetjentene ble rekruttert gjennom oppsøkende innsats fra prosjektstaben, muntlig omtale innenfor politikorpset og henvisninger fra sine politisjefer eller fylkessheriffer.
Utelukkingskriterier: Graviditet, kjente utbrudd av kreft, rullestolsbruker, en bakgrunn med psykose, omfattende psykiatrisk behandling eller selvmordsforsøk var kriteriene for utelukking.
Inkluderingskriterier: (1) Arbeid som lovens håndhever i Utah, (2) dokumentert kontakt med metamfetamin og relaterte kjemikalier gjennom lovhåndhevingsaktiviteter, og (3) påfølgende utvikling av vedvarende medisinske symptomer eller kronisk dårlig helse, var inkluderingskriteriene. Politibetjenter gav skriftlig informert samtykke til overvåkning av behandling og utfall, inkludert rapportering av samlede funn.
Legen inkluderte deltakere etter sin utstrakte fortid samt legeundersøkelser, EKG og blodanalyser (stoffskifte- og lever-undersøkelser, hepatitt B-, C- og HIV-undersøkelse, komplett telling av blodlegemer og undersøkelse av skjoldbruskkjertelen). Videre tester ble foretatt, inkludert testosteronnivåer, når direkte utspørring avslørte problemer som rettferdiggjorde evaluering. Betjenter med svekkende symptomer hadde en viss prioritet; ingen behandling ble gitt fortrinn når det gjaldt antallet meth-relaterte eksponeringer, alder, kjønn eller grad innen politiet.
Pasienter omfattet sivilspanere, narkotikaspanere og betjenter fra Special Weapons and Tactics (SWAT) fra mange by- og distrikts-jurisdiksjoner i Utah, Utah Highway Patrol (UHP), Immigration and Customs Enforcement (ICE), politibetjenter forbundet med DEA og politibetjenter utsatt under utførelsen av kjemiske laboratorieanalyser.
Behandlingen: Standard Hubbard badstuavgiftningsprosedyre. (Hubbard 1990)
EVALUERING AV RESULTATER
Symptomforandringer og livskvalitet ble vurdert ut fra bakgrunn og legeundersøkelse, oppfølgingsintervjuer og en serie med vurderinger før og etter behandling:
- RAND 36-item Short Form Health Survey (SF-36) vurderte 4-ukers helserelatert livskvalitet før behandling. RAND SF-36 testresultatmekanismen avviker fra den autoriserte til Medical Outcomes Trust, og får frem en 9-skalas profil for funksjonsevne og fysisk og mental velbefinnende. SF-36-testresultatene ble også sammenlignet før mot etter behandling, og mot RAND US-normen for voksen befolkning.
- En 50-punkts spørreundersøkelse om behandlingen av de foregående 4 ukers symptomer, sykedager og søvnmønster ble utviklet av Foundation for Advancements in Science and Education (FASE), for kliniske rammer ved bruk av Hubbard-opplegget.
- Et spørreskjema med 13 punkter om nevrotoksisitet før og etter behandlingen, basert på parametrene i Singer (2006), vurderte problemene i de forutgående 3 ukene som involverte irritabelhet, sosial tilbaketrekking, minsket motivasjon, hukommelse om det som nylig var skjedd, konsentrasjon, mental sløvhet/omtåkethet, søvnforstyrrelser, utmattelse, hyppighet og intensitet av hodepiner, seksuell dysfunksjon, nummenhet i ekstremiteter og minsket mental skarphet, uttrykt på en 0-10-skala av Likert-typen.
- Mini-Mental State Examination.
- Daglig rapportskjemaer: Et strukturert sammendrag av vesentlige tegn/resultater registrert av trent stab hver dag under behandlingen, inkludert alle uønskede påvirkninger (enten de er relatert til behandlingen eller ikke).
For trygghetsevaluering, alle negative hendelser eller forstyrrelser av behandlingsprosedyren som kommer på det daglige rapportskjemaet, og blir vurdert av legen.
RESULTATER
Behandlingens lengde og fullføringsrater
Av totalt 66 menn og 3 kvinner, med et gjennomsnitt på 44,6 år, og som begynte fortløpende og hadde en fullføringsrate på 92,8 %; fullførte 5 menn ikke behandlingen. Gjennomsnittslengden for de 64 pasientene som fullførte behandlingen, var 33 dager.
Symptomene som var tilstede hos mer enn 50 % av politibetjentene som ble registrert under påmeldingsevalueringen, inkluderte utmattelse: 96 %, søvnløshet: 91 %, hodepiner: 90 %, halsbrann: 81 %, personlighetsforandringer: 78 %, nummenhet i hender og/eller føtter: 77 %, hukommelsestap: 77 %, allergisk bakgrunn: 75 %, dårlig konsentrasjon: 75 %, ryggsmerter: 71 %, leddsmerter: 71 %, kortpustethet ved anstrengelse: 70 %, hudirritasjon: 68 %, engstelse/depresjon: 65 %, tarmluft/magesmerter: 65 %, sinusitt/tetthet: 55 % og vondt i halsen: 52 %.
Prosentdel av betjenter med unormale funn ved påmelding: De unormale funnene inkluderte forhøyet mengde av lipider (gruppe fettstoffer) i blodet: 58 %, forhøyet leverfunksjonstester: 41 %, Rombergs symptom (manglende evne til å holde balansen med bena i «tandemstilling» og uten synsinntrykk): 35 %, høyt blodtrykk: 28 %, høy blodglukose: 19 %, lavt testosteroninnhold i blodet: 17 % og lavt innhold av skjoldbruskkjertelhormoner i blodet: 17 %.
Trygghet under opplegget
Ubehag eller andre «komplikasjoner» (et uttrykk som betyr å ha emosjonelle eller sykdomslignende symptomer) forstyrret ikke leveringen av programmet vesentlig. For eksempel opplevde hver eneste deltaker forbigående rødme eller kløe, vanligvis forårsaket av niacin, men dette grep ikke forstyrrende inn i leveringen og deltakernes fullføring av programmet. Som tabell 2 viser, var det mange deltakere som opplevde temporære effekter, slik som å føle seg fortvilt, ha forbigående hoste, utmattethet osv. Disse var alle forbigående og krevde ikke legekonsultasjon. Søvnløshet endret dog av og til leveringen av programmet. Etter en natt med mindre enn fullgod søvn, ble programmet neste dag gitt i et redusert omfang. To betjenter hadde ekte gikt, og den ene avbrøt programmet.
TESTRESULTATER FRA RAND SF-36:
Forandring i helserelatert livskvalitet
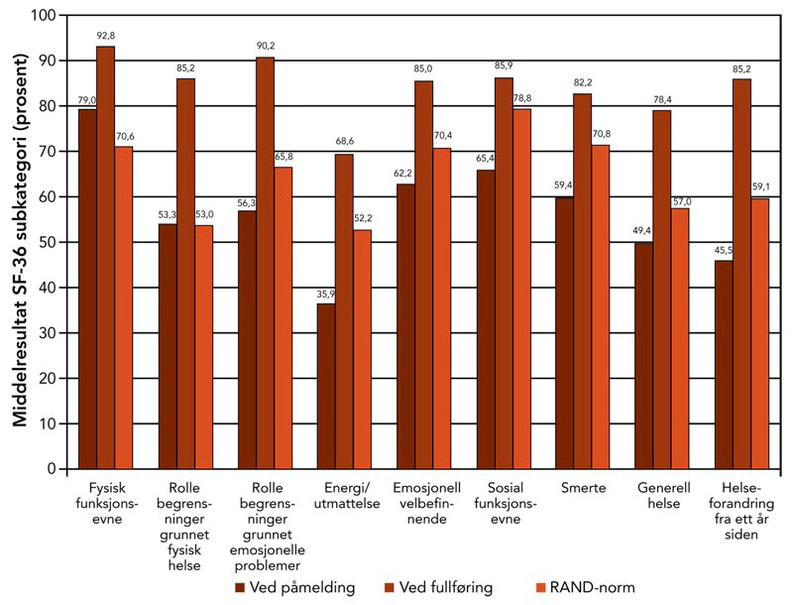
Figur 2 viser i grafisk form gjennomsnittlige SF-36-resultater før og etter behandling, kalkulert ved å bruke metodologien til RAND og sammenlignet med befolkningsnormen for De forente stater, for betjentene som fullførte opplegget.
Gjennomsnittsverdien for betjentenes poengtall for helserelatert livskvalitet, var markant lavere enn befolkningsnormen til RAND på alle 9 underskalaer, unntatt for rollebegrensninger grunnet fysisk helse og rollebegrensninger grunnet emosjonelle problemer. Etter behandlingen viste betjentenes poengtall markante statistiske forbedringer jamført med poengtall før behandlingen. Betjentenes poengtall etter behandlingen var også markant forbedret på alle underskalaer jamført med RANDs befolkningsnormer.
Symptomsintensitet og dager med dårlig helse
Gjennomsnittlige poengtall for symptomsintensitet før og etter behandling er vist i Figur 3 og er betydelig redusert etter behandlingen sammenlignet med før behandlingen.
Pasienter rapporterte om gjennomsnitt på:
- 9,3 dager med dårlig fysisk helse før behandling, forbedret til 1,8 dager ved fullføring;
- 6,3 dager med dårlig psykisk helse før behandling i forhold til 1,4 dager ved fullføring;
- 4,3 dager med begrensede aktiviteter grunnet dårlig helse før behandling i forhold til 0,2 dager ved fullføring; og
- 2,0 sykedager før behandling i forhold til 0,3 dager ved fullføring.
Søvnmønstre
Deltakerne hadde før behandlingen gjennomsnittlig 5,8 timer med søvn, noe som bedret seg til 7,6 timer ved fullføring.
Poengtall for nevrotoksisitet
Dette spørreskjemaet ble gitt til betjent nummer 20 og videre derfra. Ser vi bort fra ukomplette data, var det 38 par som passet sammen med responser før og etter behandlingen (en 84,4 % responsrate). Det gjennomsnittlige poengtallet for nevrotoksisitet før behandling var 65,5, mens poengtallet etter behandling var 14,6.
Mini-Mental Status Evaluation
På en skala som gikk til 30 poeng, indikerer poengtall under 25 betydelig kognitiv dysfunksjon. Ingen målbar forandring ble funnet med å sammenligne poengtallene før og etter behandlingen.
Drøfting
Politibetjenter behøver generelt robuste, fysiske egenskaper og emosjonell stabilitet. I kontrast til kriterier for egnethet i jobben, hadde betjenter som ble behandlet i dette prosjektet, kroniske svekkende symptomer som stemmer overens med det å være utsatt for kjemikalier.
I denne lille gruppen på 69 personer, er det overraskende at 2 delmengder på 17 % av pasientene utviste lavt innhold av skjoldbruskkjertelhormoner og/eller lav testosteron-tilstand. Utbredelsen av hypotyreose er i De forente stater på omtrent 5 %. Forutgående ubalanse av skjoldbruskkjertelhormoner kan predisponere politibetjenter for kronisk sykdom, men lav tilstand når det gjelder skjoldbruskkjertelhormoner kan være et direkte resultat av å være utsatt for metamfetaminer, med tanke på det årsaksbestemte forholdet mellom kjemikalier i omgivelsene og lav funksjon av skjoldbruskkjertelen.
De felles symptomene for dem som rapporterte kronisk dårlig helse, var også uvanlig. Mer enn 75 % av politibetjentene rapporterte alle de følgende ni symptomene: utmattelse, søvnløshet, hodepine, halsbrann, personlighetsforandringer, nummenhet i hender og/eller føtter, hukommelsestap, en bakgrunn med allergisymptomer og dårlig konsentrasjon. Denne symptomgruppen reiser muligheten for at «felles eksponeringer» kan ha utløst «felles symptomer». Dette symptommønsteret kan kanskje hjelpe kommende forskere eller utøvere innen behandling til bedre å gjenkjenne og klassifisere utsettelse for metamfetaminer. SF-36 sine poengtall for betjenter som var utsatt for metamfetaminer, indikerer mer smerte, mer utmattelse og tegn på betydelig dårligere helse enn den generelle befolkningen.
Det er i denne sammenhengen at Hubbards badstubaserte behandlingsprosedyre ble benyttet. Hvis kjemiske eksponeringer og/eller forurensning forårsaket disse kroniske symptomene, da var et «avgiftningsprogram» med mange fasetter en fornuftig tilnærming.
Så vidt vi vet, er dette første gangen et badstubasert «avgiftningsprogram» har blitt evaluert hos metamfetamin-eksponerte politibetjenter. Den store majoriteten fullførte kuren med minimalt ubehag eller ulempe, oppnådde betydelig reduksjon i sine symptomer og målbart forbedret helse og livskvalitet. Det antyder at dette programmet kunne hjelpe lignende utsatte politibetjenter andre steder.
| Antall som opplevde hendelse | Antall som gikk glipp av dager grunnet hendelse | Antall som ba om konsultasjon med lege grunnet hendelse | Antall som avbrøt programmet grunnet hendelse | ||||||
| Niacinrødme, kløende hud | 69 | 0 | 0 | 0 | |||||
| Emosjonell, irritabel, fortvilet | 18 | 0 | 0 | 0 | |||||
| Hoste, tetthet, vondt i halsen | 13 | 0 | 0 | 0 | |||||
| Influensalignende symptomer, ingen feber | 11 | 0 | 0 | 0 | |||||
| Influensalignende symptomer med lett feber | 2 | 0 | 0 | 0 | |||||
| hodepine | 6 | 0 | 0 | 0 | |||||
| Søvnløshet, livaktige drømmer | 15 | 12a | 0 | 1b | |||||
| Utmattelse | 14 | 0 | 0 | 0 | |||||
| Magekramper, kvalme, diaré | 8 | 3 | 0 | 0 | |||||
| Verk i kroppen | 5 | 2 | 0 | 0 | |||||
| Ekte gikt | 2c | 2 | 1 | 1 | |||||
| Arbeidsrelaterte eller andre konflikter i forbindelse med tidsplan | 5 | 4 | 0 | 3d | |||||
|
aIfølge prosedyren får pasienter som fikk mindre enn 6 ½ times søvn, neste dags behandling forkortet til 10 minutter med mosjon og 4 badstuperioder på 10 minutter hver, avbrutt av 10-minutterspauser. bDenne pasienten meldte om vesentlige forbedringer i helse, men fikk ikke nok søvn under programmet. Behandlingen blir betraktet som ukomplett med tanke på all dataanalyse. cBegge pasienter rapporterte om episoder med gikt før de startet på programmet. dTo betjenter satte av utilstrekkelig tid til behandling og ble nødt til å returnere til arbeidet sitt; den tredje avbrøt, viste til arbeidsrelaterte faktorer og gikk også glipp av 6 dager midt i opplegget. |
|||||||||
Referanser:
- Alexson O, Hogstedt C (1994) The health effects of solvents. In: Zenz C, Dickerson OB, and Horvath EP (eds) Occupational Medicine. St. Louis: Mosby Press, 764–768.
- Betsinger G (2006) Coping with meth lab hazards. Occupational Health and Safety 75(11): 50, 52, 54–58.
- Burgess JL (2001) Phosphine exposure from a methamphetamine laboratory investigation. Journal of Toxicology Clinical Toxicology 39(2): 165–168.
- Burgess JL, Barnhart S, and Checkoway H (1996) Investigating clandestine drug laboratories: adverse medical effects in law enforcement personnel. American Journal of Industrial Medicine 30(4): 488–494.
- Burgess JL, Kovalchick DF, Siegel EM, Hysong TA, and McCurdy SA (2002) Medical surveillance of clandestine drug laboratory investigators. Journal of Occupational and Environmental Medicine 44(2): 184–189.
- Carpenter DO, Arcaro K, and Spink DC (2002) Understanding the human health effects of chemical mixtures. Environmental Health Perspective 110(suppl 1): 25–42.
- CDC (2000) Public health consequences among first responders to emergency events associated with illicit methamphetamine laboratories—selected states, 1996–1999. MMWR Morbidity and Mortality Weekly Report 49(45): 1021–1024.
- CDC (2003) Recognition of illness associated with exposure to chemical agents—United States, 2003. MMWR Morbidity and Mortality Weekly Report 52(39): 938–940.
- CDC (2005) Acute public health consequences of methamphetamine laboratories—16 states, January 2000–June 2004. MMWR Morbidity and Mortality Weekly Report 54(14): 356–359.
- Cecchini M, LoPresti V (2007) Drug residues store in the body following cessation of use: impacts on neuroendocrine balance and behavior—use of the Hubbard sauna regimen to remove toxins and restore health. Medical Hypotheses 68(4): 868–879.
- Cecchini MA, Root DE, Rachunow JR, and Gelb PM (2006) Chemical exposures at the World Trade Center: use of the Hubbard sauna detoxification regimen to remove toxins and restore health. Townsend Letter 273: 58–65.
- Crinnion W (2007) Components of practical clinical detox programs—sauna as a therapeutic tool. Alternative Therapies in Health and Medicine 13(2): S154–S156.
- Dahlgren J, Cecchini M, Takhar H, and Paepke O (2007) Persistent organic pollutants in 9/11 World Trade Center rescue workers: reduction following detoxification. Chemosphere 69(8): 1320–1325.
- EHP Forum (1998) The threat of meth. Environmental Health Perspectives 106: A172–A173.
- Folstein MF, Folstein SE, and McHugh PR (1975) ‘‘Mini-mental state’’. A practical method for grading the cognitive state of patients for the clinician. Journal of Psychiatric Research 12(3): 189–198.
- Garwood ER, Bekele W, McCulloch CE, and Christine CW (2006) Amphetamine exposure is elevated in Parkinson’s disease. Neurotoxicology 27(6): 1003–1006.
- Hall HV, McPherson SB, Twemlow SW, and Yudko E (2003) Epidemiology. In: Yudko E, Hall HV, and McPherson SB (eds) Methamphetamine Use: Clinical and Forensic Aspects. Boca Raton: CRC Press, 13–15.
- Hays RD, Sherbourne CD, and Mazel RM (1993) The RAND 36-Item Health Survey 1.0. Health Economics 2(3): 217–227.
- Herpin G, Gargouri I, Gauchard GC, Nisse C, and Khadhraoui M, Elleuch B, et al. (2009) Effect of chronic and subchronic organic solvents exposure on balance control of workers in plant manufacturing adhesive materials. Neurotoxicity Research 15(2): 179–186.
- Hollowell JG, Staehling NW, and Flanders WD, Hannon WH, Gunter EW, Spencer CA, et al. (2002) Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). The Journal of Clinical Endocrinology and Metabolism 87(2): 489–499.
- Hubbard LR (1990) Clear Body, Clear Mind. 2002 ed. Los Angeles: Bridge Publications.
- Kilburn KH, Warsaw RH, and Shields MG (1989) Neurobehavioral dysfunction in firemen exposed to polychlorinated biphenyls (PCBs): possible improvement after detoxification. Archives of Environmental Health 44(6): 345–350.
- Leonard KL. (2008). Is patient satisfaction sensitive to changes in the quality of care? An exploitation of the Hawthorne effect. Journal of Health Economics 27(2): 444–59.
- Levisky JA, Bowerman DL, Jenkins WW, Johnson DG, and Karch SB (2001) Drugs in postmortem adipose tissues: evidence of antemortem deposition. Forensic Science International 121(3): 157–160.
- Marshall DR (2000) Report before the 106th congress: emerging drug threats and perils facing Utah’s youth. Salt Lake City, UT: Committee on the Judiciary, United States Senate. http://frwebgate.access.gpo.gov/cgi-bin/getdoc.cgi?dbname. 106_senate_ hearings&docid. f:73821.pdf (accessed 17 April 2011)
- Martyny JW, Arbuckle SL, McCammon CS, Esswein EJ, and Erb N (2004) Chemical exposures associated with clandestine methamphetamine laboratories. Denver, CO: National Jewish Medical and Research Center www.nationaljewish.org/pdf/chemical_ exposures.pdf. (accessed 17 April 2011).
- Martyny JW, Van Dyke MV, McCammon CS, Erb N, and Arbuckle SL (2005a) Chemical exposures associated with clandestine methamphetamine laboratories using the anhydrous ammonia method of production. Denver, CO: National Jewish Medical and Research Center. http://www.njc.org/pdf/Ammonia%20Meth.pdf. (accessed 17 April 2011).
- Martyny JW, Van Dyke M, McCammon CS, Erb N, Arbuckle SL (2005b) Chemical exposures associated with clandestine methamphetamine laboratories using the hypophosphorous and phosphorous flake method of production. National Jewish Medical Research Center http://www.njc.org/pdf/meth-hypo-cook.pdf (Accessed 9 Feb 2011).
- Miller MD, Crofton KM, Rice DC, and Zoeller RT (2009) Thyroid-disrupting chemicals: interpreting upstream biomarkers of adverse outcomes. Environmental Health Perspectives 117(7): 1033–1041.
- Rea WJ, Pan Y, Johnson AR, Ross GH, Suyama H, and Fenyves EJ (1996) Reduction of chemical sensitivity by means of heat depuration, physical therapy and nutritional supplementation. Journal of Nutritional and Environmental Medicine 6: 141–148.
- Schep LJ, Slaughter RJ, and Beasley DM (2010) The clinical toxicology of metamfetamine. Clinical Toxicology (Philadelphia) 48(7): 675–694.
- Schnare DW, Ben M, and Shields MG (1984) Body burden reduction of PCBs, PBBs and chlorinated pesticides in human subjects. Ambio 13: 378–380.
- Schnare DW, Denk G, Shields M, and Brunton S (1982) Evaluation of a detoxification regimen for fat stored xenobiotics. Medical Hypotheses 9(3): 265–282.
- Sharpe RM (2003) The “oestrogen hypothesis”—where do we stand now? International Journal of Andrology 26(1): 2–15.
- Singer R (2006) Neurotoxicity Guidebook. San Diego, CA: Aventine Press, 3.
- Witter RZ, Martyny JW, Mueller K, Gottschall B, and Newman LS (2007) Symptoms experienced by law enforcement personnel during methamphetamine lab investigations. Journal of Occupational and Environmental Hygiene 4(12): 895–902.
- Thrasher DL, Von Derau K, and Burgess J (2009) Health effects from reported exposure to methamphetamine labs: a poison center-based study. Journal of Medical Toxicology 5(4): 200–204.
- Tretjak Z, Beckmann S, Tretjak A, and Gunnerson C (1989) Report on occupational, environmental, and public health in Semic: a case study of polychlorinated biphenyl (PCB) pollution. In: Post-Audits of Environmental Programs and Projects; Proceedings, Environmental Impact Analysis Research Council / ASCE. New Orleans, LA, 57–72.
- Tretjak Z, Shields M, and Beckmann SL (1990) PCB reduction and clinical improvement by detoxification: an unexploited approach? Human and Experimental Toxicology 9(4): 235–244.
- Tsyb AF, Parshkov EM, Barnes J, Yarzutkin VV, Vorontsov NV, and Dedov VI (1998) Proceedings of the 1998 International Radiological Post Emergency Response Issues Conference. Washington, DC: US EPA, 162–166, efile pages 178–182. Witter RZ, Martyny JW, Mueller K, Gottschall B, and Newman LS (2007) Symptoms experienced by law enforcement personnel during methamphetamine lab investigations. Journal of Occupational and Environmental Hygiene 4(12): 895–902.
- Woodruff TJ (2011) Bridging epidemiology and model organisms to increase understanding of endocrine disrupting chemicals and human health effects. The Journal of Steroid Biochemistry and Molecular Biology 127(1–2): 108–117.
- Wu FC, Tajar A, Beynon JM, Pye SR, Silman AJ, Finn JD, et al. (2010) Identification of late-onset hypogonadism in middle-aged and elderly men. The New England Journal of Medicine 363(2): 123–135.

